리튬일차전지에 대한 이해 (리튬 염화티오닐 전지-Li/SOCl2)
안녕하세요. 공대생P 입니다. 이번 포스팅에서는 화성시 서신면 전곡리의 아리셀에서 발생한 안타까운 사고의 원인이 되는 리튬일차전지에 대해 말씀드리고자 합니다.
1. 일차전지와 이차전지에 대한 간략한 설명
전지(배터리)에 대해 처음 접하시는 분들은 이것들에 대해 헷갈릴 수 있습니다. 일차전지와 이차전지의 정의로 구분 지어 말씀드리자면 다음 내용과 같습니다.
| 구분 | 정의 |
| 1차전지 | 전기화학반응이 비가역적인 전지 (= 사용 후 재사용할 수 없는 전지) ex : 마트 건전지 |
| 2차전지 | 전기화학반응이 가역적인 전지 (= 사용 후 재사용할 수 있는 전지) ex : 핸드폰/노트북/전기차에 사용되는 전지 |
1차전지 = 재사용이 불가능
2차 전지 = 재사용이 가능
이렇게 이해하시면 빠르고 쉽게 이해하실 것이라 생각합니다.
2. 리튬-염화티오닐 전지에 대한 이해
이번 사고의 원인이 되는 Li/SOCl2 전지에 대해 알아보겠습니다. 리튬-염화티오닐 전지는 일차전지로 전기화학반응이 비가역적인 특징을 가지는 전지입니다.

아시다시피 전지(배터리)는 양극/음극/분리막/전해액 소재가 사용되며 특히 양극과 음극의 소재에 따라 전압 및 에너지밀도가 결정되는 시스템입니다. 넓은 온도 범용성에 따라 군용 및 항공등에 적용되는 것이 특징인 배터리입니다. 기존에 잘 알려진 리튬이온전지와 달리 리튬-염화티오닐 전지는 어떠한 구조를 가질까요?
2.1. 리튬-염화티오닐 배터리의 구조
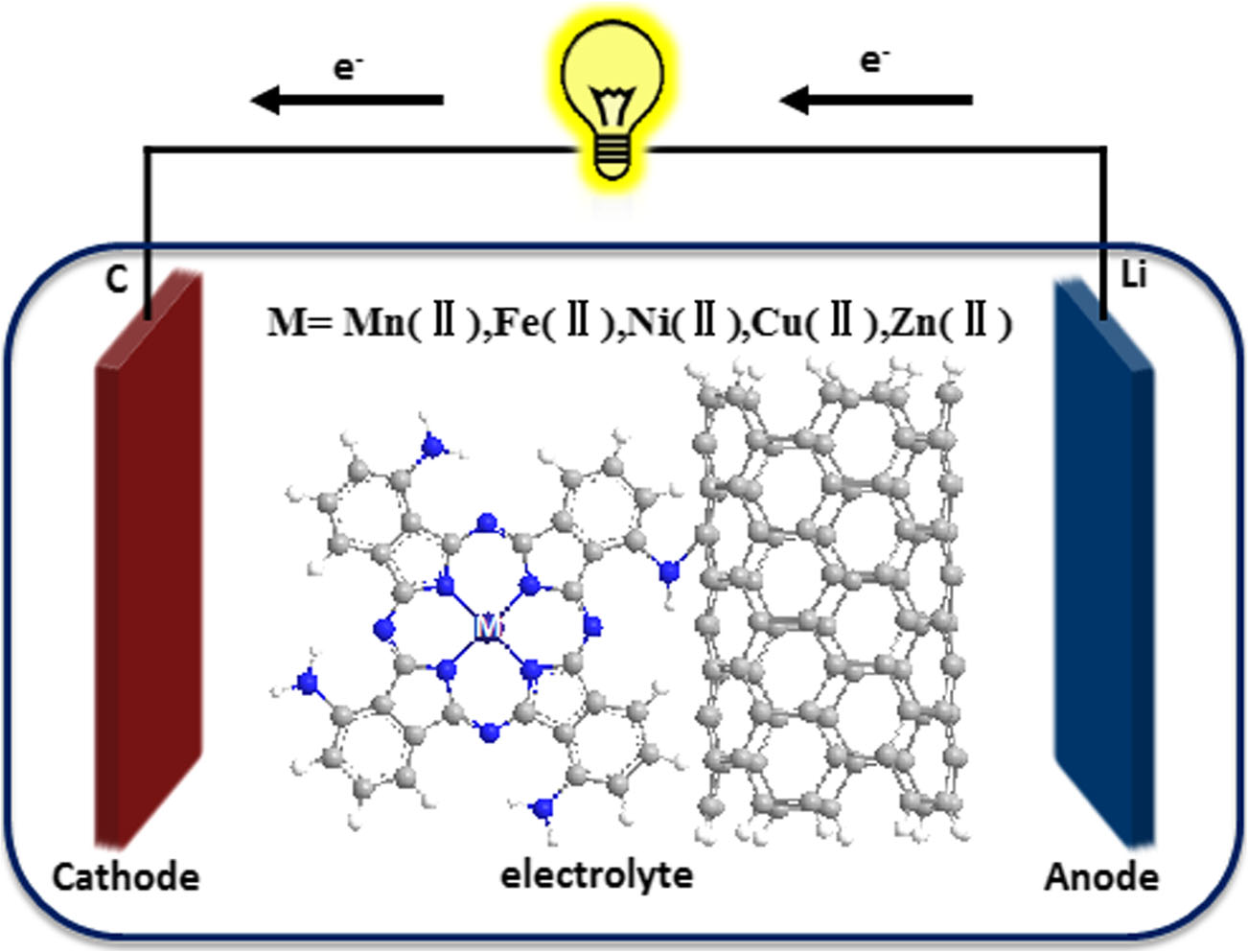
위 그림은 해당 전지에 대한 그림을 간략하게 표현한 것입니다. 해당 전지는 양극으로는 카본(탄소), 음극으로는 리튬메탈 (Li)를 사용하고 전해액으로는 LiAlCl4/SOCl2를 사용한 것이 특징입니다. 음극으로 리튬메탈을 사용하는 것이 특징입니다. (참고 : 그림에 메탈 M = Mn, Fe .. 부분은 논문에서 첨가제로 사용하는 부분이기에 무시하고 봐주셔도 됩니다.)
2.2. 리튬-염화티오닐 배터리의 방전메커니즘

그 다음으로 말씀드릴 부분은 메커니즘입니다. 일차전지이기 때문에 충전과정이 없는 것이 특징입니다. 비가역적인 반응이기 때문에 충전과정이 필요하지 않습니다. 메커니즘은 2차 전지에 비해 간단하다고 생각됩니다. 음극의 리튬메탈에서 산화반응을 통해 전자와 리튬이온이 발생합니다. 반대로 양극에서는 음극에서 발생한 전자를 받아 환원반응이 일어납니다. 이 때 염화티오닐(SOCl2)이 환원되어 염화리튬, 황, 이산화황을 생성하는 메커니즘을 갖고 있습니다.
2.3. 장점 및 단점

장점
- 높은 에너지밀도 : 작은 부피로도 높은 용량을 보유하여 에너지 밀도가 높은 편입니다.
- 온도 범용성 : 상온에서 최대 60도까지 사용되는 리튬이온전지와는 달리 약 -55 ~ 80 °C의 넓은 범용성을 지니고 있습니다.
- 높은 자가방전율 : 전지 특성 상 충전 후 전압이 점점 떨어지는 자가방전에 안정적이므로 오랜 기간 동안 전지를 사용할 수 있습니다.
단점
- 안전성 문제 : 리튬메탈을 사용하기 때문에 안전에 매우 취약합니다. 리튬메탈(Li)은 수분과 접촉 시 수소가스를 생성하며 폭발 반응을 일으키기 때문에 안전성 측면에 취약한 단점이 있습니다.
끝으로 이번 서신면 전곡리에서 발생한 사고에 대해 안타깝게 생각하며, 다시는 이같은 사고가 일어나지 않았으면 하는 바람입니다.