리튬에어배터리는 기존의 리튬이온배터리보다 10배 이상 높은 에너지밀도(약 3500 Wh/kg)를 보유하고 있는 고용량 차세대배터리이다. 충전과 방전이 연속적으로 가능한 2차전지이며, 공기(air)를 이용하여 구동되는 특징이 있다. 이러한 특징을 기반으로 활발한 연구가 이루어져왔다.
1. 구성요소
리튬에어배터리는 어느 전지들 처럼 양극과 음극이 존재하는 배터리이다. 양극으로는 대게 다공성탄소(Porous carbon)을 사용하고, 음극으로는 리튬금속(Li-metal)을 사용한다. 특이한 점은 전해액을 어떻게 사용하느냐에 따라 분리막의 유무가 달라지는 특징이 있다.

전해액은 총 4가지인 비수계(Aprotic)/수계(Aqueous)/고체전해질(Solid state)/혼합(Mixed aqueous+aprotic)등이 있다. 유기물질인 비수계의 경우 리튬금속 표면에 SEI가 형성되어 구동되고, 수계의 경우에는 음극에 인공적으로 처리를 한 Artificial interface가 형성된다. 고체 및 혼합전해질의 경우 그림과 같이 각각 다른 구조를 지닌다.
2. 작동원리
작동원리를 아래 그림을 참고하여 방전(Discharge)과정과 충전(Charge) 과정으로 구분지어 설명하고자 한다. 리튬에어배터리는 다른 전지와 다르게, 다공성탄소에 리튬이 포함되어 있지 않아 리튬금속이 에어(Air)의 산소(oxygen)과 반응하는 방전과정이 충전과정보다 먼저 일어난다.

<방전과정> 에서 음극의 리튬금속은 셀내부로 주입되는 공기에 포함되어 있는 산소와 반응하여 산화반응이 일어난다. 이때 2개의 리튬이 1개의 산소분자와 결합하여 Li2O2의 생성물을 만들어낸다. 또한 리튬금속의 산화반응에서 생겨난 전자는 도선을 따라 양극의 다공성탄소로 이동을하게 된다.
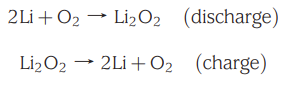
<충전과정>에서는 방전과정에서 생성된 리튬산화물(Li2O2)이 분해되어 2개의 리튬과 1개의 산소분자를 발생시키는 역반응이 나타나게 된다. 반응으로 생겨난 리튬이온은 전해액을 통해 음극의 리튬메탈로 이동하고, 기체형태의 산소를 배출하게 되는 것이다.
3. 충방전 곡선 그래프 (Voltage profile)
위 그림은 리튬에어배터리의 충방전곡선 그래프(Voltage profile)을 나타낸 것이다. 그림을 참고하여 충전곡선이 2.1~4.2V을 나타내고, 방전곡선은 3.3V~2.1V로 나타나있다.

실제 셀 구동 전압범위는 약 (2.4V~4.2V)로 리튬이온배터 (3.0V~4.2V) 보다 좀 더 넓은 범위를 갖는다. 비용량(Specific capacity)는 그래프 상 630mAh/g 으로 기존 NCM소재보다 높은 방전용량을 갖는다. 또한 리튬에어배터리의 용량을 결정짓는 양극소재가 더 비표면적이 높은 다공성소재라면 단위질량당 더 많은 리튬이온을 저장할 수 있기 때문에 비용량이 더 늘어날 수 있다고 생각된다.
리튬메탈배터리는 현재 음극으로 사용되는 리튬금속의 불안정성 및 낮은 수명의 문제 때문에 아직 상용화까지는 이르다는 의견이 대다수이다. 산소를 배출하여 친환경적이고, 여러형태의 전해질로 설계가 가능하며 고용량 에너지밀도를 구현할 수 있기 때문에 미래배터리로서 항공기 및 전기차 분야에 널리 사용될 것이라 판단된다. 공기전지가 기술발전을 통해 하루 빨리 상용화되길 바란다.
'차세대 이차전지' 카테고리의 다른 글
| 나트륨 배터리에 대한 이해와 장점과 단점 (0) | 2023.06.12 |
|---|---|
| 전고체배터리의 원리 및 장단점 (2) | 2023.03.15 |
| LG에너지솔루션의 차세대배터리 리튬황전지에 대한 이해 (0) | 2023.01.21 |
| 바나듐흐름전지 (Vanadium redox flow battery)의 장점, 단점 (0) | 2022.12.19 |
| 리튬메탈배터리(Lithium metal battery)에 대한 이해 및 덴드라이트 형성 원인 (0) | 2022.11.30 |





댓글